Loggen Sie sich in Ihr Konto ein
- Inkl. Rezeptausstellung
- Original Medikamente
- Transparenter Preis
- Inkl. Lieferung am nächsten Werktag
Erektile Dysfunktion
Holen Sie sich Potenzmittel mit einem Online-Rezept
Erektionsstörung oder erektile Dysfunktion bezeichnet die Unfähigkeit zum Aufbau oder Halten einer ausreichenden Erektion für den Geschlechtsverkehr. Erektionsstörungen betreffen Männer jeden Alters, allerdings nimmt die Häufigkeit der Sexualstörung im Alter stark zu. Erektile Dysfunktion kann psychische oder physische Ursachen haben und kann mit den richtigen Medikamenten sehr gut behandelt werden.
Bei Impotenz zögert der Betroffene trotz großem Leidensdruck oft aus Schamgefühl einen Arztbesuch hinaus oder vermeidet diesen. euroClinix bietet Ihnen die Möglichkeit, Arzneimittel wie Viagra, Cialis, Spedra, oder Levitra online zu bestellen. Hierzu füllen Sie ein medizinisches Formular mit den nötigen gesundheitlichen Daten aus, welches an unsere Ärzte weitergeleitet wird. Der Versand erfolgt durch unsere Apotheke schnell und zuverlässig in diskreter Verpackung.
Inhaltsverzeichnis
Was ist eine Erektionsstörung? Was sind die Symptome? Was sind die Ursachen der erektilen Dysfunktion? Wie kann ich Erektionsstörungen vorbeugen? Wie können Erektionsstörungen behandelt werden? Kann ich Potenzmittel rezeptfrei online kaufen? Wie kann ich rezeptpflichtige Medikamente zur Behandlung von Erektionsstörungen bei euroClinix kaufen?Verfügbare Medikamente
- Tadalafil ist ein Generikum von Cialis
- Dosierungen 5mg, 10mg und 20mg
- Wirkung hält bis zu 36 Stunden an
- Die Wirkung hält bis zu 36 Stunden an
- Enthält den aktiven Wirkstoff Tadalafil
- Dosierungen: 10mg, 20mg
- Originales Potenzmittel von Pfizer zur Behandlung von Impotenz
- Wirkung tritt nach 30 Minuten ein und hält 5 Stunden an
- Enthält den aktiven Wirkstoff Sildenafil

- Generikum des Markenmedikaments Levitra
- Niedrig dosiert: verfügbar in 5mg, 10mg & 20mg
- Wirkung hält bis zu 5 Stunden an
- Wirkt innerhalb von 30 Minuten
- Dosierungen 25mg, 50mg und 100mg
- Wirkung hält bis zu 4 Stunden an

- Medikament zur täglichen Einnahme gegen Impotenz
- Wirkt rund um die Uhr und erlaubt daher spontanen Geschlechtsverkehr
- Erhältlich in den Dosierungen 2.5mg und 5mg

- Wirkung kann schon nach 15 Minuten einsetzen
- Enthält den aktiven Wirkstoff Avanafil
- Verfügbare Dosiereinheiten: 50, 100 und 200mg
- Nebenwirkungsarmes Medikament zur Behandlung von Impotenz
- Wirkt schon nach 15-25 Minuten
- Enthält den aktiven Wirkstoff Vardenafil
- Zur Behandlung von leichter bis schwerer erektilen Dysfunktion
- Diskrete Einnahme ohne Wasserr
- Die Wirkung hält 5 Stunden an

- Enthält drei wirksame PotenzmittelED-Medikamente
- Finden Sie die Behandlung, die für Sie geeignet ist
- Lieferung am nächsten Tag mit diskreter Verpackung
Was ist eine Erektionsstörung?
Die erektile Dysfunktion bezeichnet die Unfähigkeit zum Aufbau oder Halten einer ausreichenden Erektion. Sie bezieht sich nicht auf ein einmaliges Erlebnis, bei dem Sie keine Erektion erreichen können.
Erektionsstörungen sind besonders im Alter Vertrauenswürdige Quelle Springer Fachzeitschriften mit Peer-Review Multidisziplinäre Forschung Gehe zur Quelle eine relativ häufige Sexualstörung bei Männern. So leiden über 50% der 70- bis 80-Jährigen an einer erektilen Dysfunktion. Kurzfristige Erektionsstörungen von weniger als 3 Monaten gelten nicht als erektile Dysfunktion oder Impotenz.
Was sind die Symptome?
Die Symptome unterscheiden sich von Person zu Person.
Es ist möglich, dass Sie unter erektiler Dysfunktion leiden, wenn Ihnen mehrmals Folgendes passiert:
- Ihr Penis wird nicht steif genug, um Geschlechtsverkehr zu haben
- Sie können gar keine Erektion bekommen
- Sie können eine Erektion bekommen, haben aber Schwierigkeiten, sie während dem Sex aufrecht zu erhalten
- Ihre Erektion hält nicht lange genug an, um zu ejakulieren
Ein früher Samenerguss als gewünscht ist kein Symptom einer erektilen Dysfunktion. Dies bezieht sich auf einen anderen Zustand namens vorzeitiger Samenerguss, die anders behandelt wird.
Was sind die Ursachen der erektilen Dysfunktion?
Eine Erektionsstörung hat in der Regel psychische oder körperliche Ursachen. Auch die Verstärkung von körperlichen Ursachen durch psychische Probleme wie Versagensängste kommt häufig vor.
Sehen Sie sich unser Video über die unterschiedlichen Ursachen an.

Körperliche Ursachen
Zu den körperlichen Ursachen gehören:
- Altern
- bestimmte Erkrankungen
- einige Medikamente
- bestimmte Zustände (wie Übergewicht oder das Rauchen)
Mit zunehmendem Alter sinkt Ihr Testosteronspiegel. Dadurch kann es zu einem Nachlassen der Erektionsfähigkeit kommen.
Auch einige Erkrankungen oder Medikamente lösen eventuell Impotenz und Erektionsstörungen aus.
| Erkrankungen, die erektile Dysfunktion verursachen können | Medikamente, die erektile Dysfunktion verursachen können |
|---|---|
|
|
Psychische Ursachen
Bei psychisch bedingten Erektionsstörungen kommt es trotz sexueller Erregung nicht zur Abgabe der gewünschten Nervensignale. Zu den häufigsten psychischen Ursachen von Erektionsstörungen zählen Probleme wie zum Beispiel:
- Depressionen
- Stress
- Angstzustände
- Probleme in der Beziehung
Wenn Sie sich unter Druck setzen, weil Sie sich Gedanken über Ihre Performance im Bett machen, können Sie in einen Teufelskreis angstbedingter erektiler Dysfunktion (oder Leistungsangst) geraten.
Mit anderen Worten: Je mehr Sie sich Gedanken darüber machen, keine Leistung zu erbringen, desto mehr ist Ihr Körper nicht in der Lage, zu performen.
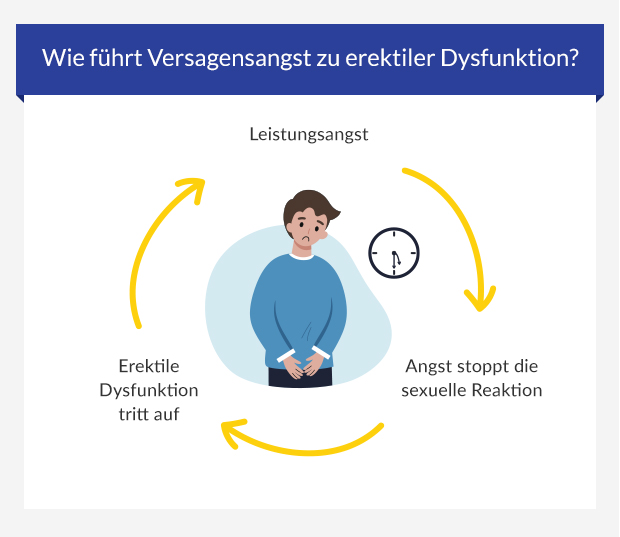
Neueste Studien haben auch Zusammenhänge zwischen Erektionsstörungen und Pornokonsum festgestellt.
Übermäßiger Konsum von Alkohol kann auch Erektionsstörungen verursachen. Auch Aktivitäten, welche die Durchblutung, die Durchblutung der Leistengegend einschränken, wie z. B. Radfahren können Ursachen sein.
Wie kann ich Erektionsstörungen vorbeugen?
Auch wenn nicht alle Arten der erektilen Dysfunktion vermeidbar sind, gibt es verschiedene Wege, eine Erektionsstörung vorzubeugen. Dazu gehören:
- ein gesunder Lebenswandel
- ausreichende Bewegung
- ausgewogene Ernährung
- Verzicht auf Zigaretten und Alkohol
Durch das Rauchen werden die Blutgefäße beschädigt und verengt, was den Blutfluss zum Penis verringert. Somit kann die Erektionsfähigkeit beeinträchtigt werden.
Durch regelmäßige sportliche Betätigung kurbeln Sie Ihre Durchblutung an.
Eine gezielte Vorbeugung gegen die erektile Dysfunktion (ED) wird mit fortschreitendem Alter schwieriger. In diesen Fällen können jedoch Potenzmittel wie Viagra oder Cialis Abhilfe schaffen.
Jüngere Männer hingegen können frühzeitig durch einen gesunden Lebensstil das Risiko für Impotenz signifikant verringern. Auch im mittleren Alter können Erektionsstörungen mit kleinen Anpassungen des täglichen Lebens erfolgreich vorgebeugt werden.
Wie können Erektionsstörungen behandelt werden?
Es gibt verschiedene Behandlungsansätze gegen die erektile Dysfunktion wie beispielsweise ein gesunder Lebenswandel oder die Einnahme von Medikamenten wie Viagra.
Natürliche Behandlungen
Es gibt viele pflanzliche Potenzmittel, die Sie ausprobieren können, bevor Sie rezeptpflichtige Medikamente einnehmen.
Dazu gehören Kräuter wie Ginseng und Maca, und werden oft als „natürliche Potenzmittel“ bezeichnet.
Sie können auch wirksame Lebensmittel gegen Erektionsstörungen in Ihre Ernährung integrieren.
Medikamente
Zur Behandlung von Erektionsstörungen kommen meist rezeptpflichtige PDE-5-Hemmer (sogenannte Phosphodiesterase-5-Hemmer) zum Einsatz.
Diese führen zu einer Erweiterung der Blutgefäße im Penis und zu einer besseren Durchblutung des Schwellkörpers. In Folge tritt eine verstärkte und verlängerte Erektion des Penis auf. PDE-5-Hemmer wirken jedoch nur bei sexueller Stimulation.
Zu den PDE-5-Hemmern zählen die folgenden Arzneimittel:
Sehen Sie sich unser Video an, in dem wir die Medikamente miteinander vergleichen:

In der folgenden Tabelle sind einige der Hauptunterschiede zwischen den vier wichtigsten Potenzmitteln aufgeführt:
|
Viagra (Sildenafil)
|
Cialis (Tadalafil)
|
|
Levitra (Vardenafil)
|
Spedra (Avanafil)
|
Kann ich Potenzmittel rezeptfrei online kaufen?
Es ist davon abzuraten, Viagra, Cialis, Levitra oder Spedra rezeptfrei im Internet zu kaufen. Auch sollten in der EU nicht zugelassene Mittel wie Kamagra vermieden werden. Im schlimmsten Fall kann sich die Erkrankung sogar verschlimmern. Bei euroClinix können Sie sich auf den unkomplizierten, diskreten und sicheren Service verlassen.
Wie kann ich rezeptpflichtige Medikamente zur Behandlung von Erektionsstörungen bei euroClinix kaufen?
Bei euroClinix können Sie durch eine einfache Online-Konsultation Potenzmittel kaufen.
Hierzu füllen Sie ein medizinisches Formular mit den nötigen gesundheitlichen Daten aus, welches umgehend an unsere Ärzte weitergeleitet wird. Diese überprüfen Ihre Angaben unter Berücksichtigung Ihrer persönlichen medizinischen Vorgeschichte. Dadurch kann die persönliche Eignung vom Medikament zur Behandlung von Impotenz festgestellt werden. Der Versand des Medikaments erfolgt unverzüglich durch die Apotheke.
- Was ist eine Erektionsstörung?
- Was sind die Symptome?
- Was sind die Ursachen der erektilen Dysfunktion?
- Wie kann ich Erektionsstörungen vorbeugen?
- Wie können Erektionsstörungen behandelt werden?
- Kann ich Potenzmittel rezeptfrei online kaufen?
- Wie kann ich rezeptpflichtige Medikamente zur Behandlung von Erektionsstörungen bei euroClinix kaufen?
Mehr lesen

Welche Erektionshilfe ist die beste für mich?
Geprüft von Dr. Caroline Fontana
Bluthochdruck und Erektionsstörungen
Geprüft von Dr. Caroline Fontana
Übungen gegen Erektionsstörungen
Geprüft von Dr. Caroline Fontana
6 Tipps zur Steigerung der Libido auf natürliche Weise
Geprüft von Dr. Caroline Fontana
Hat die Prostata einen Einfluss auf die Potenz?
Geprüft von Dr. Caroline Fontana
Kann Pornokonsum zu Erektionsstörungen führen?
Geprüft von Dr. Caroline Fontana

Mit welchen Medikamenten kann Viagra Wechselwirkungen ver...
Geprüft von Dr. Caroline FontanaArzneimittel
auswählenMedizinischen
Fragebogen ausfüllenDer Arzt stellt
Ihr Rezept ausApotheke versendet
Ihr Medikament
















